カロテノイド

自然界にみられるカロテノイド: カロテノイドは赤、橙、黄色などを示す天然色素であり、動物、植物や昆虫などに広く分布する。動物はカロテノイドを自ら生合成できないが、食物からの摂取や共生細菌による生合成などによって体内に蓄積する。
カロテノイド(カロチノイド、carotenoid)は黄、橙、赤色などを示す天然色素の一群である。
微生物、動物、植物などからこれまで750種類以上[1][2]のカロテノイドが同定されている。たとえばトマトやニンジン、フラミンゴやロブスターの示す色はカロテノイド色素による着色である。自然界におけるカロテノイドの生理作用は多岐にわたり、とくに光合成における補助集光作用、光保護作用や抗酸化作用等に重要な役割を果たす[2]。また、ヒトをはじめとする動物の必須栄養素であるビタミンAの前駆体となるほか、近年ではがんや心臓病の予防効果も報告されている[2][3]。
カロテノイドは一般に8個のイソプレン単位が結合して構成された化学式 C40H56 の基本骨格を持つ。テルペノイドの一種でもあり、テトラテルペンに分類される。ごくわずかの細菌からは、化学式C30H48を基本骨格とするものも発見されており[4]、トリテルペンに分類される。カロテノイドのうち炭素と水素原子のみで構成されるものはカロテン類、これに加えて酸素原子を含むものはキサントフィル類に分類される。カロテンの名称はニンジン(carrot)から得られた不飽和炭化水素(ene)に、キサントフィルの名称は黄色い(xantho)葉(phyll)の色素にそれぞれ由来する[3]。
カロテノイドの色素としての性質は、その分子骨格にそってのびる長い共役二重結合(ポリエン)によるものである。その共役系の長さによって、400から500 nm の間に極大をもつ異なる吸収スペクトルを示すことにより、黄色、橙色、赤色の異なる色を呈する。また、カロテノイドのもつ高い抗酸化作用もこの共役二重結合に由来する。
目次
1 生合成経路
1.1 基質であるゲラニルゲラニル二リン酸の生合成経路
1.2 フィトエンからリコペンまでの生合成経路
1.3 各種の末端が修飾されたカロテノイドの生合成経路
2 主な化合物
2.1 カロテン類
2.1.1 αカロテン
2.1.2 βカロテン
2.1.3 γカロテン
2.1.4 δカロテン
2.1.5 リコペン
2.2 キサントフィル類
2.2.1 ルテイン
2.2.2 ゼアキサンチン
2.2.3 カンタキサンチン
2.2.4 フコキサンチン
2.2.5 アスタキサンチン
2.2.6 アンテラキサンチン
2.2.7 ビオラキサンチン
3 出典
4 関連項目
5 外部リンク
生合成経路
高等植物の色素体および一部の細菌は、糖などの栄養から中心代謝経路を経て自らカロテノイドを生合成することができる。動物はカロテノイド生合成経路をもたないが、食物から摂取したカロテノイドを代謝し、ビタミンAなどをつくる。本項目では色素体や細菌内でのカロテノイド生合成経路について述べる。
基質であるゲラニルゲラニル二リン酸の生合成経路
まず、メバロン酸経路または非メバロン酸経路によってイソペンテニル二リン酸(IPP)とジメチルアリル二リン酸(DMAPP)が生合成される。どちらの経路によってIPPおよびDMAPPを生合成するかは、それぞれの生物に依存する(植物の色素体や、多くのグラム陰性菌は非メバロン酸経路をもつ一方で、赤色酵母や黄色ブドウ球菌などの微生物はメバロン酸経路をもつ)。その後、DMAPPにIPPが順次縮合されることにより、ゲラニル二リン酸(GPP)、ファルネシル二リン酸(FPP)を経て、カロテノイドの直接の基質であるゲラニルゲラニル二リン酸(GGPP)が生成される。
フィトエンからリコペンまでの生合成経路
2分子のGGPPが縮合され、安定な反応中間体であるプレフィトエン二リン酸を経て、カロテノイドの基礎骨格となる炭素数40のフィトエンが生成される。フィトエンの中心には3つの共役した二重結合があるが、内側の単結合から順に不飽和化(脱水素化)されることにより共役系が2つずつ伸びてゆき、フィトフルエン、ζ-カロテン、ニューロスポレン、リコペンが生成される[5]。リコペンまでの生合成経路は多くの生物で共通であるが、この後の生合成経路はそれぞれの生物によって大きく異なる。
各種の末端が修飾されたカロテノイドの生合成経路
リコペンの末端の環化により各種環化カロテノイドができる。リコペンを基質として、リコペンβ環化酵素が1回作用するとγ-カロテンが、2回作用するとβ-カロテンが生成される。リコペンε環化酵素が1回作用するとδ-カロテン、2回作用するとε-カロテンが生成される。リコペンβ環化酵素とリコペンε環化酵素がそれぞれ1回ずつ作用するとα-カロテンが生成される。
β-カロテンを基質としてケト化・水酸化酵素が作用することにより、β-クリプトキサンチン、ゼアキサンチン、エキネノン、カンタキサンチン、3-ヒドロキシエキネノン、3'-ヒドロキシエキネノン、アドニザンチン、フェニコキサンチン、アスタキサンチンが生成される。
そのほか、配糖化酵素・エポキシ化酵素など多くの酵素と生合成経路が同定されている。また、酵素や生合成経路が同定されていないカロテノイドも多く存在する。
主な化合物
カロテン類
αカロテン
αカロテン(あるふぁ-、α-carotene)は化学式 C40H56、分子量 536.87 のカロテン。IUPAC命名法では β,ε-カロテンとなる。CAS登録番号は 7488-99-5。融点 185.5 ℃(真空封管)の濃紫色プリズム晶。[α]64318{displaystyle {rm {left[alpha right]_{643}^{18}}}}![{rm {left[alpha right]_{{643}}^{{18}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f690bf271094e710fc11c1e725a14ab04d3ca1c1)
生物内ではγカロテンによって作られ緑黄色野菜のみならず、多くの植物にみられる。水にはほとんど溶けない脂溶性の物質で、純物質は紫色をしている。体内で酸化されレチノイドとなるが、βカロテンに比べると効力が低いとされている。
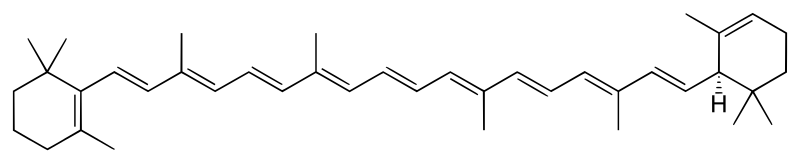
βカロテン
βカロテン(べーた-、β-carotene)は、化学式 C40H56 の植物のもつ黄色色素。IUPAC命名法では β,β-カロテンと呼ばれる。CAS登録番号は 7235-40-7。融点 183 ℃(真空封管)の濃紫色六方プリズム晶。極大吸収 (CHCl3) 497, 466nm。
かつてはドイツ語を由来としたβ-カロチンという語でも言い表された。

細胞膜の損傷を防ぐ働きをする。胃癌や肺癌に対する予防効果が注目されていたが、その効果を否定する臨床試験の結果がでた。
人体の脂肪組織に蓄えられ、肝臓や小腸の粘膜の中で、必要な時にβ-カロテンが2分子に分かれビタミンAになるため、プロビタミンAとも呼ばれる。
- β-カロテンを多く含む食べ物
緑黄色野菜 : カボチャ、ニンジン(西洋系)、アシタバ、コマツナ、シソ、ホウレンソウ、マンゴー
γカロテン
γカロテン(がんま-、γ-carotene)は化学式 C40H56、分子量 536.87 のカロテン。IUPAC命名法では β,ψ-カロテンとなる。CAS登録番号は 472-93-5。結晶多形を持ち、天然型は融点 177.5 ℃のわずかに濃い赤色プリズム晶、極大吸収 (CHCl3) 508.5, 475, 446 nm。または融点 152–153 ℃の赤色板状晶、極大吸収(エーテル)494, 462 nm。
生物内ではリコペンの異性化、βゼアカロテンの脱水素化によって作られる。水にはほとんど溶けない脂溶性の物質。αカロテンやβカロテンの前駆体として人参等に存在するが微量。ビタミンA効力は低い。

δカロテン
δカロテン(でるた-、δ-carotene)は化学式 C40H56 のカロテン。IUPAC命名法では ε,ψ-カロテンとなる。CAS登録番号は 472-92-4。融点 140.5 ℃の橙赤色針状晶。[α]D25{displaystyle {rm {left[alpha right]_{D}^{25}}}}![{rm {left[alpha right]_{{D}}^{{25}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/909c437558af53c911c9e740dcbf0773bbc251c6)
人参などの緑黄色野菜に含まれている。ビタミンA効力はかなり低い。脂溶性なので、有機溶媒で抽出しクロマトグラフィーで単離する。

リコペン
リコペン(Lycopene, lycopene、ドイツ語読みでリコピン)は化学式 C40H56、分子量 536.87 のカロテノイド。水にはほとんど溶けない脂溶性の赤色色素[6]。多くの植物ではβカロテンやαカロテンの前駆体としてわずかに存在するのみであるが、トマトや柿、金時ニンジン、グミなどに多量に存在する。抗酸化作用が大きいと考えられている。

- ε-カロテン

キサントフィル類
ルテイン
ルテイン (lutein) は分子式 C40H56O2、ジヒドロキシ-αカロテンに相当する。また、狭義にはルテインを指してキサントフィル (xanthophyll) と称することもある。CAS登録番号 127-40-2。色は黄色で、高い抗酸化作用を持ち、緑黄色野菜、果物に多く含まれる。カナリアの羽毛の黄色色素でもある。極大吸収 (CO2) 445, 475, 508 nm。
人間の目(黄斑部、水晶体)、乳房、子宮頸部にも含まれる。
目の機能強化、白内障や加齢黄斑変性などの眼病予防に役立つとして、近年注目されている。
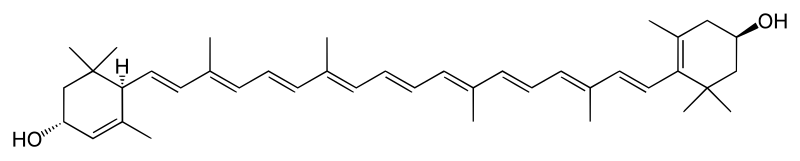
- ルテインを多く含む食物
緑黄色野菜 : ホウレンソウ - ブロッコリー - キャベツ
- 豆類
花 : マリーゴールド
藻類 : アオサ
- 卵黄
ゼアキサンチン
ゼアキサンチン (zeaxanthin) は分子式 C40H56O2、ジヒドロキシ-βカロテンに相当する。CAS登録番号 144-86-3。融点 215 ℃の黄色長板状晶。吸収極大 (CS2) 517, 482, 450 nm。
トウモロコシの種子、卵黄に含まれる。
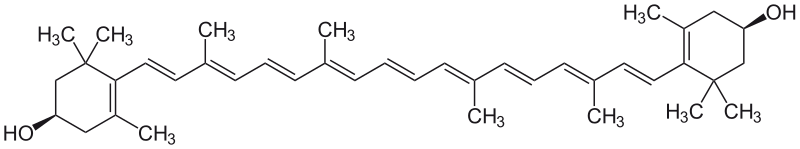
カンタキサンチン
カンタキサンチン (canthaxanthin) は分子式 C40H52O2、beta,beta-carotene-4,4'-dioneに相当する。CAS登録番号 514-78-3。融点209℃。吸収極大470~476nm。1950年食用キノコ(Cantharellus cinnabarinus)中に含まれていることが見出され、フラミンゴ等の赤色羽毛中やサケ、マスの肉中、伊勢海老からも検出されている。色調は赤色で、高い抗酸化力があり抗腫瘍作用、免疫賦活作用等のデータが示されている。

フコキサンチン
フコキサンチン(Fucoxanthin)は分子式 C42H58O6 で表される。褐藻やその他の不等毛藻に存在して茶色-オリーブ色を呈するとともに、葉緑体において光合成の補助色素として機能している。フコキサンチンは可視光線のうち青緑色から黄緑色(350-550nm)の波長域を吸収し、448nm 付近に吸収極大を持つ。

アスタキサンチン
アスタキサンチン(Astaxanthin, Astaxanthine)は分子式 C40H52O4 で表される。甲殻類の殻やそれらを餌とするマダイの体表、またサケ科魚類の筋肉の赤色部分などに見られる。生体内では遊離型、モノエステル型、ジエステル型の3形態が可能であるが、多くは脂肪酸エステル型であり、血漿リポタンパク質と結合した形で存在する。甲殻類ではタンパク質(オボルビン、クラスタシアニン)と結合し、カロテノプロテインとして存在している。タンパク質と結合したアスタキサンチンは黒っぽい青灰色を呈するが、加熱によりタンパク質分子が変性してアスタキサンチンが遊離すると、本来の赤色を呈する。甲殻類を茹でると赤くなるのはこの現象に由来する。
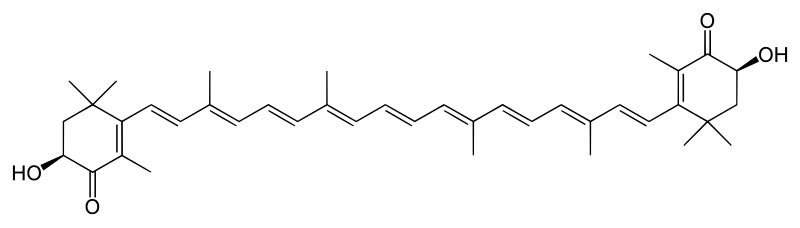
アンテラキサンチン
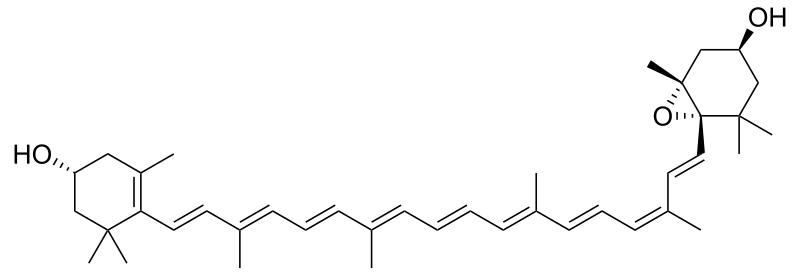
ビオラキサンチン
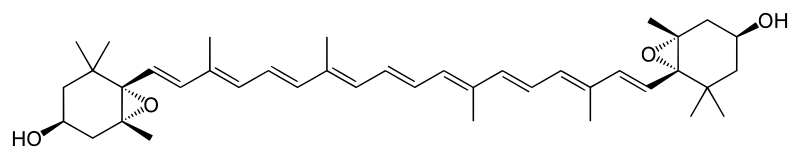
出典
^ Britton G; Liaaen-Jensen S; Pfander H (2004). Carotenoids, Handbook. Birkhäuser Basel. doi:10.1007/978-3-0348-7836-4. ISBN 978-3-7643-6180-8. http://www.springer.com/us/book/9783764361808.
- ^ abc三室 守、高市真一、富田純史 『カロテノイド―その多様性と生理活性―』 高市真一 編、裳華房、2006年。ISBN 978-4-7853-5840-2。
- ^ ab眞岡孝至『カロテノイドの多様な生理作用』食品・臨床栄養、2、2007年。
^ Tao, L. (2005年). “Novel carotenoid oxidase involved in biosynthesis of 4,4'-diapolycopene dialdehyde.”. Appl Environ Microbiol 71: 3294-3301.
^ Sandmann, G. (2009年). “Evolution of carotene desaturation: The complication of a simple pathway”. Arch Biochem Biophys 483: 169-174. http://www.ncbi.nlm.nih.gov/pubmed/18948076.
^ Kuti, Joseph O.; Konuru, Hima B. (2005年). “Effects of genotype and cultivation environment on lycopene content in red-ripe tomatoes”. Journal of the Science of Food and Agriculture 85: 2021–2026. doi:10.1002/jsfa.2205. http://lib3.dss.go.th/fulltext/Journal/J.Sci.Food%20and%20Agri/2005v85/no.12/2005v85no12p2021-2026.pdf.
関連項目
栄養学 - 栄養素
外部リンク
カロテノイド - (オレゴン州大学・ライナス・ポーリング研究所)
β-カロテン(横浜市衛生研究所 - 食品衛生情報)
カロテン - 「健康食品」の安全性・有効性情報(国立健康・栄養研究所)
リコピン - 同
ルテイン - 同- キエビネの花の細胞中のカロチノイド
- 日本カロテノイド研究会
| ||||||||||||||||
| ||||||||||
| ||||