アルケン
この記事は検証可能な参考文献や出典が全く示されていないか、不十分です。 出典を追加して記事の信頼性向上にご協力ください。(2018年10月) |

最も単純なアルケン、エテン(エチレン)の空間充填モデル
アルケン(ドイツ語: Alken、英語: alkene)は化学式 CnH2n (n≧2) で表される有機化合物で、C-C間の二重結合を1つ持つ。すなわち、不飽和炭化水素の一種。エチレン系炭化水素、オレフィン (olefin)、オレフィン系炭化水素とも呼ばれる。C-C二重結合を構成している2つπ結合1つとσ結合1つから成り立っており、このうちπ結合の結合エネルギーはC-H結合のものよりも小さく、付加反応が起こりやすい。例えばエテン(エチレン)と塩素の混合物に熱を与えると 1,2-ジクロロエタンが生成する。
目次
1 アルケン類の命名
1.1 慣用名の「オレフィン」
1.2 IUPAC命名法
1.3 慣用名
2 主なアルケン
3 生成
4 反応
4.1 付加(還元)反応
4.1.1 触媒を用いる水素化反応
4.1.2 アルケンに対するH-Xの求電子付加反応
4.1.3 求核水和反応
4.1.4 ハロゲン分子の求電子付加
4.1.5 ヒドロホウ素化
4.1.6 四酸化オスミウムによる隣接シンジヒドロキシ化
4.1.7 シクロプロパン環の生成
4.1.8 ペリ環状反応
4.1.9 オキシ水銀化-脱水銀化
4.2 重合反応
4.3 酸化反応
4.4 遷移金属を触媒とするC−C結合生成反応
5 脚注
6 関連項目
アルケン類の命名
慣用名の「オレフィン」
古くから、ある種の気体は塩素を作用させると油状の物質が得られることから、ラテン語の「油(羅: oleum)」に因み、このような気体を「生油気、オレフィン・ガス(英: olefiant gas)」と呼んでいた。この気体はエチレンであることが判り、炭素の二重結合を持つ炭化水素をオレフィン系炭化水素、単にオレフィン、またはエチレン系炭化水素と総称していた。[1]
IUPAC命名法
IUPAC命名法によるアルケン類の系統名は、対応するアルカン (alkane) の語尾 -ane を -ene に変化させるだけの単純なものである。例えば、対応するアルカンがエタン (ethane) CH3−CH3 の場合、アルケン CH2=CH2 はエテン (ethene) となります。
二重結合の位置の異なる異性体(二重結合異性体)を持つ、及び置換基のあるアルケンについての命名法は以下の規則に従う。
- 二重結合を含む最も長い炭素鎖を主鎖とする。単結合だけならばより長い炭素鎖がありえたとしても、それを主鎖と認めない。
- 二重結合の炭素の位置番号は、最も小さくなるように振る。
- 二重結合の位置を、2つの炭素のうち小さいほうの位置番号で示す。シクロアルケンの場合、二重結合の位置は1番か2番と決まっているので、二重結合の位置を示す数を名前につけない。また、どちらの末端から数えても二重結合の位置が同じなら、主鎖を沿って初めに出会う置換基の番号がより小さい末端を1とする。
二重結合は自由に回転しないため、二重結合の炭素それぞれが互いに異なる2つの置換基を持っている場合、立体異性体が生じる。例えば、1,2-2置換エテンの場合、以下の2つの立体異性体があり得る。

1位と2位に1つずつ置換基を持つ置換エテン(エチレン)の異性体
上図左のように、置換基が同じ側に並んでいる立体配置をシス (cis)、右のように、置換基が違う側に位置している立体配置をトランス (trans) と呼ぶ。これは二置換シクロアルカンのシス、トランスと同様である。直線で表す表記法では以下のように表すことができる。

二重結合のシス-トランス異性体。
これら立体化学だけが異なるアルケンの異性体をシス-トランス異性体という。シス-トランス異性体はジアステレオマーである。上図に明らかなように、シス-トランス異性体をもつ最小のアルケンは、2-ブテンである。二重結合の炭素が置換基を3つ以上有していた場合、E/Z表記法で区別する。まずカーン・インゴルド・プレローグ順位則により二重結合の炭素それぞれに存在する置換基を別々に順位付ける。そして二重結合の炭素それぞれのより優先順位の高い置換基どうしの位置関係からEかZであると決定する。すなわち、それらの置換基がシス体のように隣り合っているならば Z 配置、トランス体のように向かいにあるなら E 配置と表記する。
 |  |
| (Z)-1-ブロモ-1,2-ジフルオロエテン | (E)-2,3-ジメチルヘプタ-2-エン |
基官能命名法において、官能基を持つアルケンでは、主鎖及び末端の決定に、官能基が二重結合よりも大きな影響力を持つ。例えばヒドロキシ基を持つアルケンは、二重結合を持つアルコールと解釈され、「アルケノール」と命名される。アルケノールの主鎖はヒドロキシ基と二重結合を両方とも含まねばならない。また、番号付けはヒドロキシ基の番号が小さくなる方を採用する。
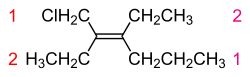
枝分かれや置換基を持つアルケンはアルカンと同様の方法で命名する。二重結合の位置は、アルキル基の位置に優先する。
 |  | |
| ヘキサ-1-エン | 4-メチルヘキサ-1-エン | 2-エチル-4-メチルヘキサ-1-エン |
慣用名
アルケンはIUPAC命名法による名称とは別に慣用名を持つことがある。以下に例を示す。
CH2=CH2{displaystyle {{ce {CH2=CH2}}}} | CH3CH=CH2{displaystyle {{ce {CH3CH=CH2}}}} | CH3C(CH3)=CH2{displaystyle {{ce {CH3C(CH3)=CH2}}}}  | |
| IUPAC名: | エテン | プロペン | 2-メチルプロペン |
| 慣用名: | エチレン | プロピレン | イソブテン、イソブチレン |
主なアルケン
エチレン(エテン) n = 2, C2H4
プロピレン(プロペン) n = 3, C3H6
ブテン n = 4, C4H8
ペンテン n = 5, C5H10
ヘキセン n = 6, C6H12
ヘプテン n = 7, C7H14
オクテン n = 8, C8H16
ノネン n = 9, C9H18
デセン n = 10, C10H20
生成
アルカンのクラッキング。
アルコールを160–170 ºCで分子内脱水して得られる。アルコールの分子内脱水はザイツェフ則に従う。
ハロゲン化アルキルに強塩基を加えるとハロゲン化水素の脱離反応によってアルケンが得られる。これもザイツェフ則に従う。アルコールからスルホン酸エステルを経由して脱離反応によりアルケンを得る手法も一般的である。脱離反応は他に4級アンモニウムを基質とするホフマン脱離、アミンオキシドを基質とするコープ脱離、ほかシュガエフ脱離、セレノキシド脱離、ランバーグ・バックランド反応など。- アルケンは、C-C二重結合のそれぞれの炭素についている2つの置換基がそれぞれ異なる場合、E 型(トランス型)と Z 型(シス型)の幾何異性体を持つ。これらを選択的に合成するにはアルキンからの変換反応を用いると便利である。リンドラー触媒を用いてアルキンを還元すると Z 型のアルケンが、バーチ還元の条件でアルカリ金属を作用させると E 型のアルケンが得られる。
アルデヒドやケトンとアルキリデン化試薬とのカップリング反応。ウィッティヒ反応、ホーナー・ワズワース・エモンズ反応、ピーターソン反応、ジュリア・リスゴーオレフィン化、テッベ試薬など。マクマリー反応は2個のカルボニル基からアルケンを作る。
反応
付加(還元)反応
アルケンの付加反応はC-C二重結合が求電子剤によって求電子攻撃されることから始まり、最終的にC-C二重結合が単結合になる反応である。すなわち、求電子付加反応である。反応の条件や用いる試薬によって、経緯は様々であるが、一般的に反応剤X-Yの単結合が切断され、それぞれ異なる二重結合の炭素に付加する。
下図に反応式の例を示す。

X-Yのエチレン(エテン)への付加
触媒を用いる水素化反応
水素の付加によってC-C二重結合を飽和させ単結合とする反応。C-C二重結合を水素化するには触媒が必要である。水素は二重結合の炭素にsyn付加する。立体障害が少ない面が選択される。触媒は不均一系または均一系のいずれかである。溶媒によく用いられるのはメタノール、エタノール、酢酸、酢酸エチルなど。
触媒がなければ、H-H結合(結合解離エネルギー 104kcal/mol)を切断するのは困難である。熱的に水素分子を切断することは不可能といえるほど困難であり、水素分子は電気的に中性なので二重結合の求電子攻撃を受けない。そのため、アルケンの水素化は発熱反応であるが、高温でも起こらない。多く用いられる触媒はパラジウム、白金、ニッケルなどの不溶な物質である。不均一触媒の役目は表面に水素原子と結合し、晒すことである。
触媒を用いる水素化はsyn選択的に起こる。触媒表面に水素分子が結合すると、表面に水素原子が隣接する。C-C二重結合はまず一方のH-触媒表面結合を求電子攻撃し、触媒表面に求核攻撃する。その後、C-触媒表面 はまだ触媒表面に結合している水素に求核置換反応し、水素化は終わる。syn選択性は水素原子の付加が触媒表面という一つの側に限定されることによる。二重結合の面の上側と下側のどちらに付加するは、立体障害が十分少ないなら等価なのでラセミ体が生じ、立体障害があるなら障害が少ない側からのみ起こるので光学異性体が生じる。
アルケンに対するH-Xの求電子付加反応
C-C二重結合にプロトンH+が付加してできるカルボカチオンの安定性が議論される。二重結合の炭素のうち、電子供与基の多いものにXが、電子求引基の多いものにHが付加する。
求核水和反応
C-C二重結合に対する、求核剤X、求電子剤Yからなる化合物X-Yの付加反応を考える。Xの求核性が乏しく、溶媒に水などの求核剤を採用していた場合、Yによって生じたカルボカチオンにXではなく溶媒が作用する。求核水和反応 (nucleophilic hydration) はこれの溶媒が水の場合におこる反応であり、アルコールを与える。
ハロゲン分子の求電子付加
ハロゲン分子X-Xの付加反応は触媒なし、非求核性溶媒中で1,2-ジハロゲン化物を生じる。このとき、anti付加体が生じる。ハロゲンのうち、塩素Cl2と臭素Br2はうまく反応する。フッ素F2は反応が激しすぎて扱いが難しく、ヨウ素I2は熱力学的に不利である。
ハロゲン分子は水素分子同様、電気的に中性であるが、その共有結合は分極しやすく、求核剤があるとヘテロリシス開裂する。以降、臭素分子Br2とアルケンの付加反応について話を進める。 C-C二重結合のπ電子が臭素分子を求核攻撃し、一方の炭素にBrと付加する。このときのカルボカチオンは環状のブロモニウムイオンであり、臭素が二重結合の炭素に架橋し、三員環が生じる。引き続く、このブロモニウムイオンに対する求核攻撃は、橋架けしているBr原子とは反対側の面に限られるため、anti選択性が生じる。
ヒドロホウ素化
四酸化オスミウムによる隣接シンジヒドロキシ化
四酸化オスミウムを化学量論的に用いるか、N-メチルモルホリン N-オキシド (NMO) 等の第二の酸化剤(犠牲試薬)と組み合わせて触媒量用いることで、アルケンをsyn-1,2-ジオールに変換できる。
シクロプロパン環の生成
ペリ環状反応
オキシ水銀化-脱水銀化
アルコールやエーテルの合成に用いられる。マルコフニコフ則が適用され、転位反応が起こらない。
重合反応
チーグラー・ナッタ触媒を使った付加重合反応によるポリアルケン(ポリエチレンやポリプロピレン)の生成。
酸化反応
過酸、過酸化水素を用いて酸化するとエポキシドが生成する。対応する不斉反応として香月・シャープレス酸化、史不斉エポキシ化がある。シャープレス不斉ジヒドロキシ化はキラルな1,2-ジオールを与える。
- オゾン分解
オゾンで酸化した後に還元的/酸化的に処理するとC-C二重結合が切れて2本のC-O二重結合に置き換わり、2分子のカルボニル化合物を与える。
ワッカー酸化は工業的にも重要な酸化反応である。
臭素などを付加させた後に、水酸化カリウムなどによる二段階の脱ハロゲン化水素を経てアルキンへと変換される。アルコールや酢酸イオンの存在下に臭素やヨウ素を作用させるとハロゲンと酸素官能基の1,2-付加体が得られる。
遷移金属を触媒とするC−C結合生成反応
- 遷移金属を触媒とする結合形成反応。オレフィンメタセシス反応、ヘック反応など。オキソ法は工業的に重要。
脚注
^ “コトバンク - 世界大百科事典「アルケン」”. 2018年9月23日閲覧。
関連項目
- 不飽和炭化水素
- アルカン
- アルキン
- カルベン
| ||||
